INTRODUCCIÓN
El estado gaseoso de la materia, se caracteriza porque los átomos o moléculas se encuentran muy separados entre sí y sus interacciones son mucho más débiles que en el estado líquido y sólido. Las moléculas de los gases se mueven libremente chocando contra las paredes del recipiente que los contiene, lo que origina la presión del gas. Cuanto mayor sea la temperatura, mayor será la velocidad de las moléculas, y por lo tanto, mayor debe ser el volumen para que la presión no varíe. Mediante este trabajo se darán a conocer las diferentes leyes de la química. En este informe se dará a conocer algunos conceptos sobre los gases y algunas reacciones que se presentaran en yenka.
OBJETIVOS
Reforzar los conocimientos previos acerca de los gases.
Conocer y diferenciar las leyes de gases.
Conocer las propiedades de los gases.
Saber ante qué circunstancias se debe aplicar cada Ley.
Conocer y diferenciar los diversos conceptos de gases
MARCO TEÓRICO
El estado gaseoso es un estado disperso de la materia, es decir, que las moléculas del gas están separadas unas de otras por distancias mucho mayores del tamaño del diámetro real de las moléculas. Resuelta entonces, que el volumen ocupado por el gas depende de la presión, la temperatura y de la cantidad o numero de moles.
1. Se adaptan a la forma y el volumen del recipiente que los contiene. Un gas, al cambiar de recipiente, se expande o se comprime, de manera que ocupa todo el volumen y toma la forma de su nuevo recipiente.
2. Se dejan comprimir fácilmente. Al existir espacios intermoleculares, las moléculas se pueden acercar unas a otras reduciendo su volumen, cuando aplicamos una presión.
3. Se difunden fácilmente. Al no existir fuerza de atracción intermolecular entre sus partículas, los gases se esparcen en forma espontánea.
4. Se dilatan, la energía cinética promedio de sus moléculas es directamente proporcional a la temperatura aplicada
Variables que afectan el comportamiento de los gases
1. PRESIÓN
Es la fuerza ejercida por unidad de área. En los gases esta fuerza actúa en forma uniforme sobre todas las partes del recipiente.
La presión atmosférica es la fuerza ejercida por la atmósfera sobre los cuerpos que están en la superficie terrestre. Se origina del peso del aire que la forma. Mientras más alto se halle un cuerpo menos aire hay por encima de él, por consiguiente la presión sobre él será menor.
2. TEMPERATURA
Es una medida de la intensidad del calor, y el calor a su vez es una forma de energía que podemos medir en unidades de calorías. Cuando un cuerpo caliente se coloca en contacto con uno frío, el calor fluye del cuerpo caliente al cuerpo frío.
La temperatura de un gas es proporcional a la energía cinética media de las moléculas del gas. A mayor energía cinética mayor temperatura y viceversa.
La temperatura de los gases se expresa en grados kelvin.
3. CANTIDAD
La cantidad de un gas se puede medir en unidades de masa, usualmente en gramos. De acuerdo con el sistema de unidades SI, la cantidad también se expresa mediante el número de moles de sustancia, esta puede calcularse dividiendo el peso del gas por su peso molecular.
4. VOLUMEN
Es el espacio ocupado por un cuerpo.
5. DENSIDAD
Es la relación que se establece entre el peso molecular en gramos de un gas y su volumen molar en litros.
Gas Real
Los gases reales son los que en condiciones ordinarias de temperatura y presión se comportan como gases ideales; pero si la temperatura es muy baja o la presión muy alta, las propiedades de los gases reales se desvían en forma considerable de las de gases ideales.
Concepto de Gas Ideal y diferencia entre Gas Ideal y Real.
Los Gases que se ajusten a estas suposiciones se llaman gases ideales y aquellas que no, se les llaman gases reales, o sea, hidrógeno, oxígeno, nitrógeno y otros.
- Un gas está formado por partículas llamadas moléculas. Dependiendo del gas, cada molécula está formada por un átomo o un grupo de átomos. Si el gas es un elemento o un compuesto en su estado estable, consideramos que todas sus moléculas son idénticas.
- Las moléculas se encuentran animadas de movimiento aleatorio y obedecen las leyes de Newton del movimiento. Las moléculas se mueven en todas direcciones y a velocidades diferentes. Al calcular las propiedades del movimiento suponemos que la mecánica newtoniana se puede aplicar en el nivel microscópico. Como para todas nuestras suposiciones, esta mantendrá o desechara, dependiendo de sí los hechos experimentales indican o no que nuestras predicciones son correctas.
- El número total de moléculas es grande. La dirección y la rapidez del movimiento de cualquiera de las moléculas pueden cambiar bruscamente en los choques con las paredes o con otras moléculas. Cualquiera de las moléculas en particular, seguirá una trayectoria de zigzag, debido a dichos choques. Sin embargo, como hay muchas moléculas, suponemos que el gran número de choques resultante mantiene una distribución total de las velocidades moleculares con un movimiento promedio aleatorio.
- El volumen de las moléculas es una fracción despreciablemente pequeña del volumen ocupado por el gas. Aunque hay muchas moléculas, son extremadamente pequeñas. Sabemos que el volumen ocupado por una gas se puede cambiar en un margen muy amplio, con poca dificultad y que, cuando un gas se condensa, el volumen ocupado por el gas comprimido hasta dejarlo en forma líquida puede ser miles de veces menor. Por ejemplo, un gas natural puede licuarse y reducir en 600 veces su volumen.
- No actúan fuerzas apreciables sobre las moléculas, excepto durante los choques. En el grado de que esto sea cierto, una molécula se moverá con velocidad uniformemente los choques. Como hemos supuesto que las moléculas sean tan pequeñas, la distancia media entre ellas es grande en comparación con el tamaño de una de las moléculas. De aquí que supongamos que el alcance de las fuerzas moleculares es comparable al tamaño molecular.
- Los choques son elásticos y de duración despreciable. En los choques entre las moléculas con las paredes del recipiente se conserva el ímpetu y (suponemos) la energía cinética. Debido a que el tiempo de choque es despreciable comparado con el tiempo que transcurre entre el choque de moléculas, la energía cinética que se convierte en energía potencial durante el choque, queda disponible de nuevo como energía cinética, después de un tiempo tan corto, que podemos ignorar este cambio por completo.
Leyes de los gases ideales
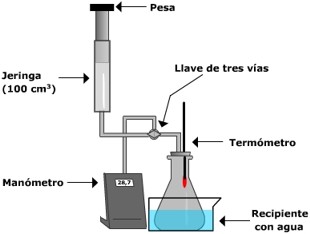
La Ley de Boyle, formulada por Robert Boyle y Edme Mariotte, es una de las leyes de los gases ideales que relaciona el volumen y la presión de una cierta cantidad de gas mantenida a temperatura constante. La ley dice que el volumen es inversamente proporcional a la presión:
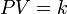
Donde 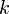 es constante si la temperatura y la masa del gas permanecen constantes.
es constante si la temperatura y la masa del gas permanecen constantes.
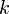 es constante si la temperatura y la masa del gas permanecen constantes.
es constante si la temperatura y la masa del gas permanecen constantes.
Cuando aumenta la presión, el volumen disminuye, mientras que si la presión disminuye el volumen aumenta. No es necesario conocer el valor exacto de la constante 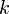 para poder hacer uso de la ley: si consideramos las dos situaciones de la figura, manteniendo constante la cantidad de gas y la temperatura, deberá cumplirse la relación:
para poder hacer uso de la ley: si consideramos las dos situaciones de la figura, manteniendo constante la cantidad de gas y la temperatura, deberá cumplirse la relación:
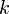 para poder hacer uso de la ley: si consideramos las dos situaciones de la figura, manteniendo constante la cantidad de gas y la temperatura, deberá cumplirse la relación:
para poder hacer uso de la ley: si consideramos las dos situaciones de la figura, manteniendo constante la cantidad de gas y la temperatura, deberá cumplirse la relación: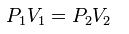
Donde:
La Ley de Charles
Es una de las leyes de los gases ideales. Relaciona el volumen y la temperatura de una cierta cantidad de gas ideal, mantenido a una presión constante, mediante una constante de proporcionalidad directa. En esta ley, Charles dice que para una cierta cantidad de gas a una presión constante, al aumentar la temperatura, el volumen del gas aumenta y al disminuir la temperatura el volumen del gas disminuye. Esto se debe a que la temperatura está directamente relacionada con la energía cinética (debida al movimiento) de las moléculas del gas. Así que, para cierta cantidad de gas a una presión dada, a mayor velocidad de las moléculas (temperatura), mayor volumen del gas.
La ley de Charles es una de las leyes más importantes acerca del comportamiento de los gases, y ha sido usada en muchas aplicaciones diferentes, desde para globos de aire caliente hasta en acuarios. Se expresa por la fórmula:
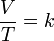
Donde:
- V es el volumen
- T es la temperatura absoluta (es decir, medida en Kelvin)
- k es la constante de proporcionalidad.
- 1 matraz Erlenmeyer de 250 ml.
- 1 vaso precipitado de 2000 ml.
- 1 vaso de precipitado de 1000 ml.
- 3 cilindros graduados de 100,500 y 1000 ml.
- 1 termómetro.
- 2 soportes universales.
- 1 pinza tipo nuez.
- 1 pinza de extensión
- 1 bureta de 50 ml.
- 1 regla de 30 cm o cinta métrica.
- 1 chicle
- 2 planchas de calentamiento
- Pinza para bureta
- 2 globos
- Etanol
- Fósforos
- Zinc
- Ácido clorhídrico
PRACTICAS EN EL LABORATORIO YENKA
- PRUEBAS DE LLAMA
- Cloruro de litio
- Cloruro de potasio
- Carbonato de sodio
PREGUNTAS
respuesta:
a) Bario
PRUEBAS DE GASES
- Dioxido de carbono
- Hidrogeno
- Oxigeno
CONCLUSIONES
- Se pudo ver y aclarar la reacción de las diferentes sustancias químicas a la llamadel mechero de bunsen.
- Se logró adquirir mayor habilidad en el manejo del mechero de bunsen y susdiferentes características.
- Se pudo determinar que cuando la llama del mechero de bunsen se alimenta deoxigeno esta es más eficiente (llama azul).
- Se puede decir que las leyes de Charles y Boyle Mariott son muy importantes en nuestra Química ya que cada una tiene su pensamiento.
- Reconocimos aprendiendo las técnicas de separación aplicando sus diferentes métodos de cada ingrediente.
WEBGRAFIA
- http://www.juntadeandalucia.es/averroes/recursos_informaticos/andared02/leyes_gases/
- http://www.educaplus.org/gases/gasesreales.html
Se pudo determinar que cuando la llama del mechero de bunsen se alimenta de
Se pudo ver y aclarar la reacción de las diferentes sustancias químicas a la llamadel mechero de bunsen
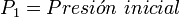
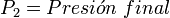
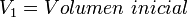
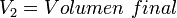





















BUEN TRABAJO 5,0
ResponderEliminar